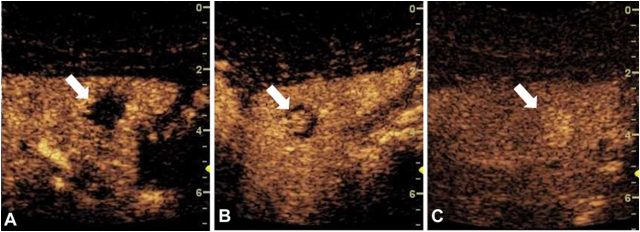
近期梅奥诊所的 Tefferi 教授对骨髓增生反常归纳征的确诊、预后评价以及医治进行了总述,发表于 AJH 的 40 周年纪念刊上。
确诊
1. 确诊规范
2007 年的维也纳会议提出了骨髓增生反常归纳征(MDS)的最低确诊规范,从形态学、细胞遗传学、免疫表型、集落培育等方面归纳确诊。需求留意的是血细胞削减、骨髓病态造血、环形铁粒幼细胞(RS)以及染色体反常、原始细胞增多等并非 MDS 的特有体现,应留意辨别。
其次,确诊规范中骨髓三系病态造血阈值一致设定为大于 10% 值得商讨,有研讨标明针对各系应有不同规范。最终,MDS-EB 需与 MDS 转化的 AML(AML-MRC)相辨别。如有 50% 以上红系病态造血且原始细胞少于 19%,考虑 MDS-EB,大于 20% 则应该考虑 AML-MRC。
2. 分型
1982 年提出 FAB 规范,依据患者外周血和骨髓病态造血、原始细胞份额、环形铁粒幼细胞(RS)数量以及外周血单核细胞数量,将 MDS 分为 5 型:难治性贫血(RA)、环形铁粒幼细胞性难治性贫血(RAS)、难治性贫血伴原始细胞增多(RAEB)、难治性贫血伴原始细胞增多向白血病转变型(RAEB-t)、缓慢粒-单核细胞性白血病(CMML)。
2001 年 WHO 将 CMML 归为 MDS/MPN,MDS-RAEB-t 归为白血病,MDS-RAEB 进一步分为 RAEB-I(原始细胞 5%~10%)以及 RAEB-II(原始细胞 11%~20%)。
2008 年 WHO 将 MDS 分为两类:原始细胞小于 5% 包含 MDS-RCUD, MDS-RARS, MDS-RCMD,5q- 归纳征,MDS-U。原始细胞大于 5% 包含 MDS-RAEB-I(外周血原始细胞<5%,骨髓 5%~9%),MDS-RAEB-II(外周血原始细胞 5%~19%,骨髓 10%~19%)。
这些提议或许会归入往后的 MDS 分型: SF3B1 骤变的 MDS 患者,只需有 RS 存在,不管多少都应归为 MDS-RARS 或许 MDS-RCMD-RS。MDS-RCMD-RS 从 MDS-RCMD 中分出作为独自的亚型。5q-兼并非高危的细胞遗传学反常或兼并 TP53 骤变患者预后欠安应注重 。
此外,达不到 MDS 确诊规范而确诊为 ICUS 患者中,经过流式细胞仪检测粒系老练反常符号,如 CD13、CD16 表达以及 CD34+细胞的免疫表型等有助于确诊。总归,基因骤变、骤变负荷以及反常免疫表型可为缺少清晰形态学特征患者中供给确诊头绪。
遗传学
1. 细胞遗传学
约 45%~51% 的患者有细胞遗传学反常,最常见的单一核型反常为 del(5q),+8,-Y,del(5q) ,-7 等,杂乱核型反常约为 9%-11%。
2. 分子遗传学
跟着二代测序的开展,在 MDS 中发现的再现性基因骤变首要有:表观调控:TET2、ASXL1、EZH2、DNMT3A、IDH1/2),RNA 剪切:SF3B1、SRSF2、U2AF35、ZESR2,DNA 批改:TP53,转录调控:RUNX1、BCOR、ETV6,信号转导:CBL,NRAS,JAK2,粘连蛋白复合物:STAG2。
提示预后欠安的有:ASXL1、EZH2、DNMT3A、RUNX1、BCOR、ETV6、CBL,NRAS;对预后无影响的有:JAK2、STAG2;仍有争议的有:TET2、IDH1/2、SRSF2、U2AF35、ZESR2、SF3B1(或许预后杰出)。
预后评分体系
1997 年 Greenberg 等人提出 IPSS 评分体系以评价 MDS 患者预后,2007 年结合 WHO 确诊规范,在 IPSS 的基础上提出了 WPSS 评分体系,2012 年 Greenberg 等人在剖析了近 7000 例 MDS 患者后提出了 IPSS-R 评分,这类评分均是在原发 MDS 患者仅承受支撑医治基础上得出的。IPSS-R 评分以及 MD Anderson 肿瘤中心提出 MDAS 评分在医治相关 MDS 及承受过疾病批改医治的患者中适用。此外,还有确诊低危组患者的 LR-MDAS 评分。
医治
1. 贫血
约 90% 的患者在病程中呈现贫血,常常需求输血支撑。首要医治如下:
红细胞生成刺激剂(ESAs)
在低危组 MDS 患者中,ESAs 总反响率为 40%-50% ,中位有用时刻 2 年,未承受输血患者中效果较好。在血红蛋白<100 g/L 且 EPO<500 的患者中可考虑运用。ESAs 应固定剂量而非依据体重核算剂量。栓塞、癫痫以及充血性心力衰竭等不良反响不常见。额定的 G-CSF 医治与单用 ESAs 效果无异。
达那唑
Chabannon 等人报导达那唑(600 mg/d)医治 CR 为 26%,而梅奥诊所一项研讨标明达那唑(800 mg/d)无效,故达那唑是否有用仍有争议。
免疫按捺疗法(IST)
低增生性 MDS 患者(骨髓安排活检有核细胞增生程度<30%(70 岁以下)或<20%(60 岁以上)),往往有免疫功用紊乱,与再障相似。在兼并 PNH 克隆的低增生性 MDS 患者中,有报导称 ATG 联合环孢素医治的总反响率达 50%,HLA-DRB1-15 阳性患者对 IST 反响更好。
雷那度胺
雷那度胺经过按捺酪氨酸激酶起效,FDA 同意用于 MDS 兼并 5q-。Lisa 等人的研讨中,5q-、二倍体核型以及其他核型的患者对雷那度胺的反响率分别为 83%、57%、12%。常见不良反响包含中性粒细胞削减及血小板削减,均为剂量相关。
综上,若对 ESAs、达那唑以及雷那度胺均不灵敏,可考虑去甲基化医治或参与临床实验。TGF-β/SMAD 信号通路的靶向药物,如 ACE-011 以及 ACE-536 很有远景,而端粒酶按捺剂 imetelstat 效果不及 ESAs。
2. 铁过剩
铁过剩影响患者生计,低危及中危-I 的 MDS 患者若输注大于 20~30 单位的红细胞且血清铁蛋白>1000~2500μg/L,可考虑行去铁医治,但由于肾脏及消化道不良反响发生率较高,并不主张对一切患者惯例行去铁医治。
3. 血小板削减
血小板削减在对折中危、低危-I 的 MDS 患者中呈现,且血小板功用不全还会引起出血风险增加,重复输注血小板易引起无效输注。TPO 受体激动剂如罗米司亭(rmoiplostim)虽可削减输注及出血事情,但出于或许促进白血病转化的忧虑,不主张用于血小板削减的 MDS 患者中。
4. IPSS-R 评分低危组(极低危、低危以及中危-I 组)
主张在有症状的血细胞削减呈现之前仅定时调查。别的,兼并 EZH2 以及 TP53 骤变的患者预后较差,需特别留意。
5. IPSS-R 评分中危-II 及以上组
除造血干细胞移植以外,尚无治好性药物面世。FDA 同意 5-氮杂胞苷用于 IPSS 各风险组患者。CALGB 9221 关键性临床实验中,较支撑医治而言,5-氮杂胞苷总反响率高且白血病转化的中位时刻较长。虽总生计时刻无差异,但日子质量显着改进。AZA001 实验标明在高危患者中总生计时刻也有改进。
地西他滨可用于 IPSS 分型中危-I 及以上的患者。MD Anderson 的一项 III 期临床实验标明 15 mg/m2q8 h d1~d3 的地西他滨 CR 率为 9%。ADOPT 实验中 20 mg/m2d1~d5 的 CR 率为 17%,而 EORTC-LG 实验中 3 天低剂量地西他滨医治的患者无生计方面的获益。
综上,鉴于去甲基化药物的生计获益有限,引荐 IPSS-R 评分中危-II 及以上组中无法承受 ASCT 的患者可承受临床实验(图 1)。
图 1 依照 IPSS-R 风险分层的医治战略
6. 疾病开展
耐药/复发的患者预后极差,承受化疗序贯 ASCT 是最佳挑选。关于不能耐受患者,部分处于临床实验的新药,如组蛋白去乙酰化酶按捺剂等或许有用。
7. 造血干细胞移植
有适宜供体、共患病指数且小于 70 岁患者可考虑承受 ASCT 医治。关于 ASCT 的机遇,Cutler CS 等人的研讨标明低危以及中危-I 组患者在疾病开展后移植能改进预后,而中危-II 及以上组患者前期移植能改进预后。预处理计划方面,Koreth 等人的研讨标明中危-II 及以上组患者更能从 RIC 预处理计划中获益。
总的来说,MDS 分子遗传学中的发现正影响着确诊、预后以及靶向医治的开展,等待有更多新药的临床实验成果。